Univ.-Prof.in Mag.a Dr.in Petra Heffeter, MAS
Gruppenleiterin
T: +43 (0)1 40160-57594
petra.heffeter@meduniwien.ac.at
ORCID: 0000-0001-6401-8646
Forschungsschwerpunkt
Chemotherapie und Therapie mit kleinen zielgerichteten Molekülen sind zwei Hauptstrategien für die Therapie von menschlichem Krebs im disseminierten Stadium. In den letzten Jahrzehnten wurden Tausende von Verbindungen entwickelt und haben folglich eine verbesserte Therapiewirksamkeit.
Doch selbst bei Einsatz neuer zielgerichteter Therapeutika ist eine solche Therapie oft durch starke Nebenwirkungen, Resistenzentwicklung und unzureichende Tumorakkumulation limitiert.
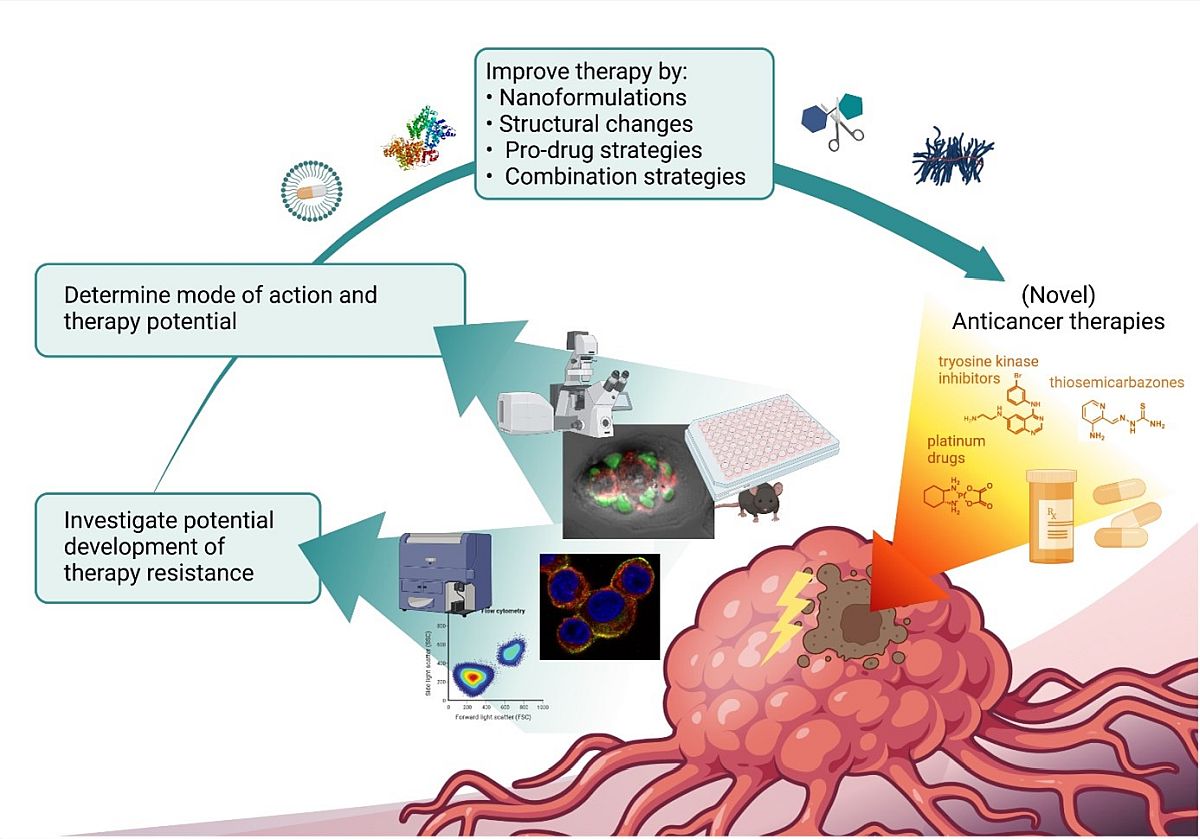
Die Forschung dieser Gruppe konzentriert sich auf die Entwicklung mehrerer neuer Strategien zur Überwindung dieser Einschränkungen:
- Verbesserung der Antikrebsaktivität durch intelligente Arzneimittelkombinationen;
- Entwicklung neuer Targeting-Strategien zur Erhöhung der Wirkstoffabgabe an das Tumorgewebe (in Kooperation mit dem Institut für Anorganische Chemie, Wien im Rahmen der „Forschungsplattform Translational Cancer Therapy Research“);
- Untersuchung der Mechanismen, die der Empfindlichkeit/Resistenz von Krebszellen gegenüber neuen Krebsmedikamenten zugrunde liegen, um das Patient:innenkollektiv zu definieren, das am meisten von einer Chemotherapie profitiert.
Ausgewählte Publikationen
Albumin-targeting of an oxaliplatin-releasing platinum(iv) prodrug results in pronounced anticancer activity due to endocytotic drug uptake in vivo
Schueffl H, Theiner S, Hermann G, Mayr J, Fronik P, Groza D, van Schonhooven S, Galvez L, Sommerfeld NS, Schintlmeister A, Reipert S, Wagner M, Mader RM, Koellensperger G, Keppler BK, Berger W, Kowol CR, Legin A, Heffeter P*.
Chem Sci. 2021 Aug 26;12(38):12587-12599. doi: 10.1039/d1sc03311e.
This publication was also awarded by the CCC best paper award in 2021 (to SH).
Cancer Cell Resistance Against the Clinically Investigated Thiosemicarbazone COTI-2 Is Based on Formation of Intracellular Copper Complex Glutathione Adducts and ABCC1-Mediated Efflux
Bormio Nunes JH, Hager S, Mathuber M, Pósa V, Roller A, Enyedy ÉA, Stefanelli A, Berger W, Keppler BK, Heffeter P* (shared last author), Kowol CR.
J Med Chem. 2020 Nov 25;63(22):13719-13732. doi: 10.1021/acs.jmedchem.0c01277.
High copper complex stability and slow reduction kinetics as key parameters for improved activity, paraptosis induction and impact on drug-resistant cells of anticancer thiosemicarbazones
Hager S, Pape VFS, Pósa V, Montsch B, Uhlik L, Szakács G, Tóth S, Jabronka N, Keppler BK, Kowol CR, Enyedy EA, Heffeter P*.
Antioxid Redox Signal. 2020 Aug 20;33(6):395-414. doi: 10.1089/ars.2019.7854.
The thiosemicarbazone Me2NNMe2 induces paraptosis by disrupting the ER thiol redox homeostasis based on protein disulfide isomerase inhibition
Hager S, Korbula K, Bielec B, Grusch M, Pirker C, Schosserer M, Liendl L, Lang M, Grillari J, Nowikovsky K, Pape VFS, Mohr T, Szakács G, Keppler BK, Berger W, Kowol CR, Heffeter P*.
Cell Death Dis. 2018 Oct 15;9(11):1052. doi: 10.1038/s41419-018-1102-z.
Bacterial Ghosts as Adjuvant to Oxaliplatin Chemotherapy in Colorectal Carcinomatosis
Groza D, Gehrig S, Kudela P, Holcmann M, Pirker C, Dinhof C, Schueffl HH, Sramko M, Hoebart J, Alioglu F, Grusch M, Ogris M, Lubitz W, Keppler BK, Pashkunova-Martic I, Kowol CR, Sibilia M, Berger W, Heffeter P*.
Oncoimmunology. 2018 Feb 16;7(5):e1424676. doi: 10.1080/2162402X.2018.1424676.
Alle Publikationen
Vorstellung Walter Berger, Petra Heffeter

Nach der Aktivierung werden Daten an YouTube übermittelt. Weitere Infos hier: Datenschutzerklärung
Förderungen
- AWS Prize 2015
- Fonds der Stadt Wien für innovative interdisziplinäre Krebsforschung
- Herzfelder'sche Familienstiftung
- Initiative Krebsforschung