Immunmodulation bei Entzündungen und Krebs
Unser Labor ist daran interessiert, die molekularen Mechanismen zu verstehen, die zu entzündlichen Erkrankungen und Krebs führen, wobei die Maus als Modellsystem verwendet wird. Wir untersuchen die zellspezifische Rolle der EGFR-Signalgebung in Krebs- und Tumorstromazellen und deren komplexe Interaktion.
Darüber hinaus wollen wir verstehen, wie myeloische Entzündungszellen die Entzündung, Tumorentwicklung und -regression beeinflussen und neue Konzepte nutzen, um Tumore so zu modulieren, dass sie empfindlicher für aktuelle Krebsbehandlungen werden.
Das ultimative Ziel ist es, dieses Wissen über die Mechanismen der Tumorentstehung auf Patient:innen zu übertragen, um wirksamere personalisierte Behandlungen für Krebs beim Menschen zu entwickeln.
EGFR-Signalweg bei der Krebsentstehung und Entzündung
EGFR-Überexpression oder -Mutationen sind in vielen menschlichen Tumoren epithelialen und glialen Ursprungs vorhanden, und gezielte Anti-EGFR-Therapien werden derzeit zur Krebsbehandlung eingesetzt. Bis vor kurzem war die tumorfördernde Funktion des EGFR ausschließlich mit seiner Expression in Tumorzellen verbunden.
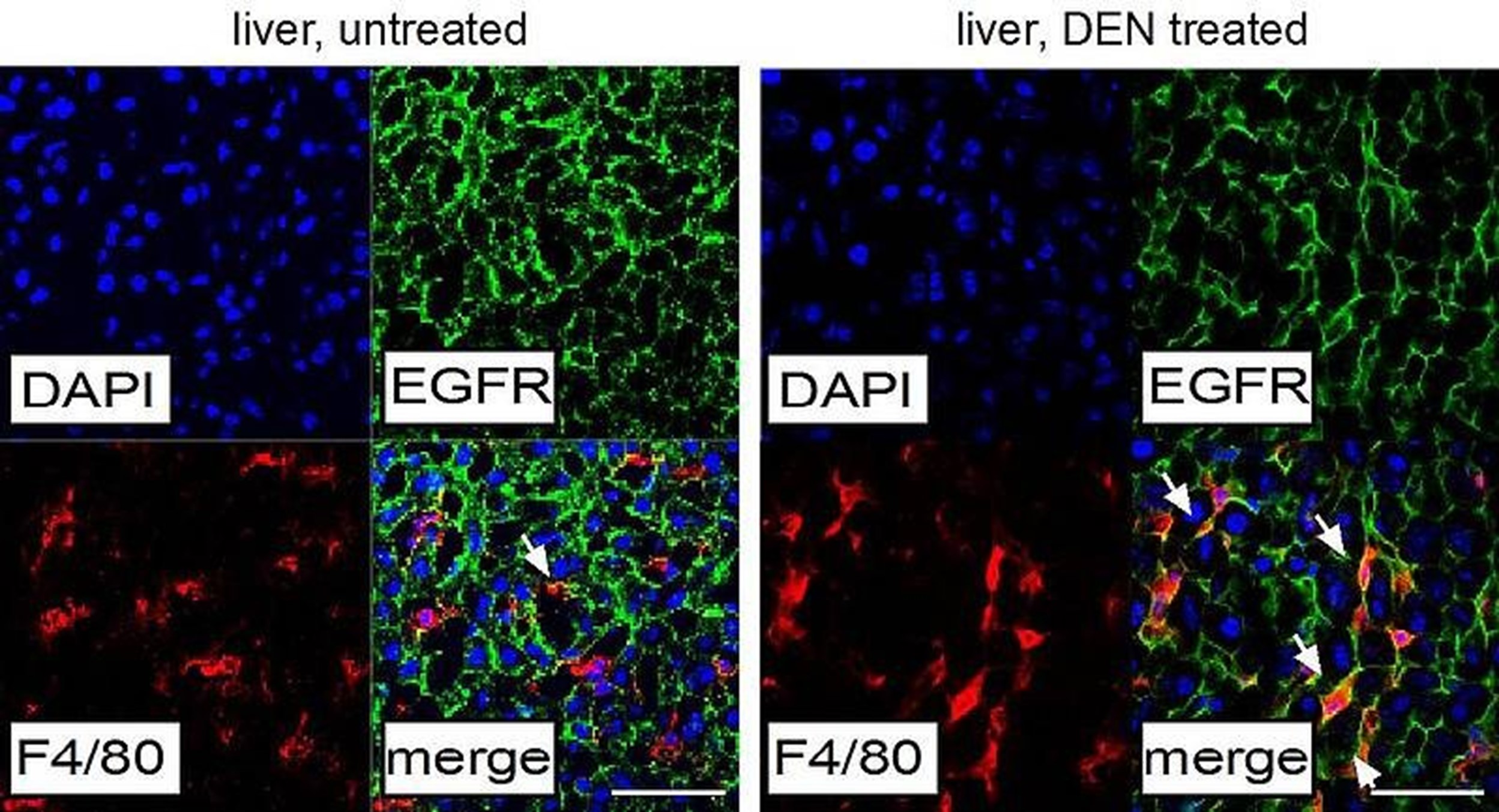
Unser Labor hat entdeckt, dass EGFR in Lebertumoren (HCC) in Lebermakrophagen (auch Kupffer-Zellen genannt) hochreguliert ist (Abbildung 1), wo er eine tumorfördernde Funktion hat, indem er die Expression von Zytokinen wie IL-6 reguliert. Durch den Einsatz gentechnisch veränderter Mausmodelle (GEMMs) haben wir gezeigt, dass die Deletion von EGFR in Makrophagen die Entwicklung von Leberkrebs drastisch reduziert, während die Deletion von EGFR in Tumorzellen sogar das Tumorwachstum beschleunigt.
Auch bei HCC-Patient:innen konnten wir zeigen, dass das Vorhandensein von EGFR-positiven Makrophagen ein schlechter prognostischer Faktor für das krankheitsfreie und Gesamtüberleben der Patient:innen ist. Diese tumorpromovierende Funktion von EGFR in anderen als den Tumorzellen ist für die Präzisionsonkologie sehr wichtig, da sie eine bessere Stratifizierung und effektivere Behandlung von Leberkrebspatient:innen ermöglicht, für die es noch keine therapeutischen Optionen gibt (Lanaya et. al. Nature Cell Biology, 2014).
Eine ähnliche Beobachtung wurde beim menschlichen CRC gemacht, wo wir EGFR-positive myeloische Zellen in der Tumormikroumgebung entdeckten, was mit einem schlechten Überleben bei metastasierten Patient:innen korrelierte. In CRC-Mausmodellen haben wir gezeigt, dass die EGFR-Hemmung in myeloischen Zellen das Tumorwachstum reduziert, während die therapeutische Deletion von EGFR in Tumorzellen dies nicht tut (Srivatsa, et al. Gastroenterology. 2017 Jul;153(1):178-190).
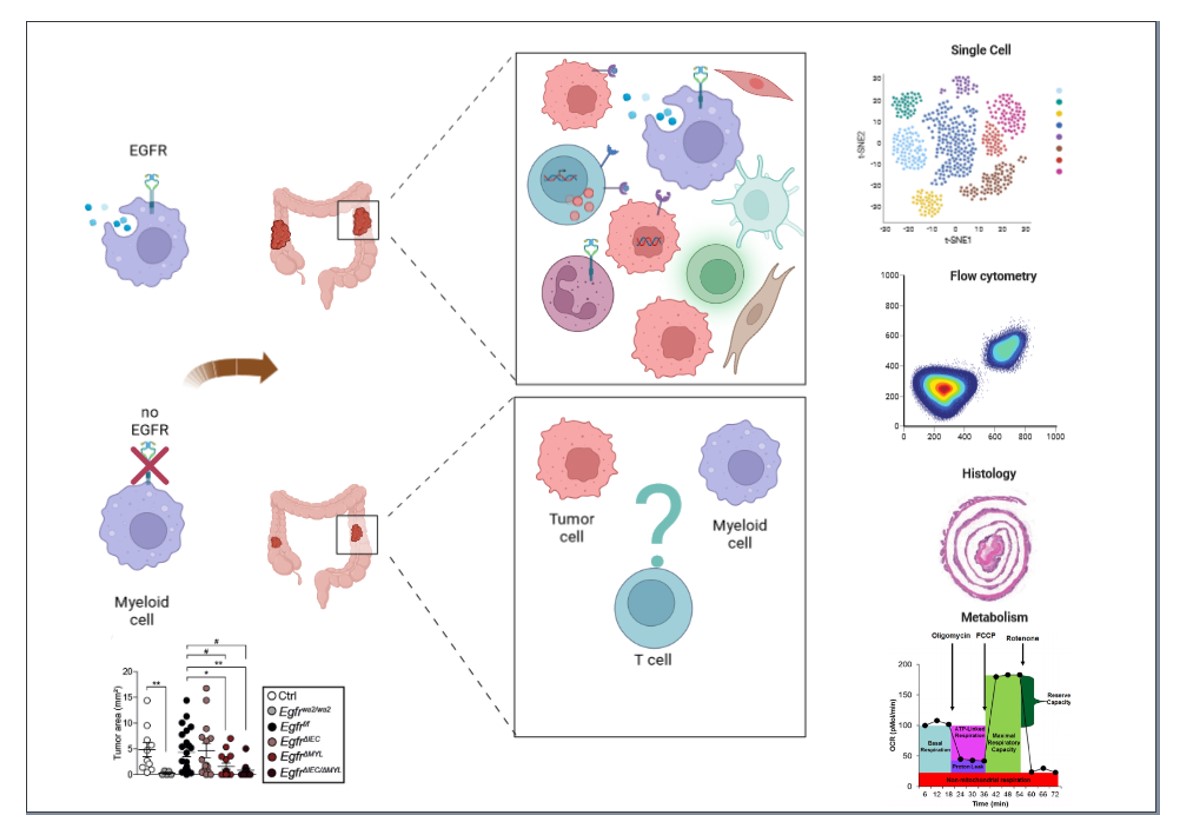
Diese Ergebnisse zwingen uns, den Mechanismus, durch den Anti-EGFR-Medikamente bei Tumoren wirksam sind, neu zu bewerten. In weiterführenden Analysen untersuchen wir, in welchen myeloischen Zellen genau der EGFR bei der Tumorentwicklung eine Rolle spielt. Dabei wollen wir die immunologischen und metabolischen Signalkaskaden, die vom EGFR beeinflusst werden identifizieren verstehen, ob und wie die Interaktion mit anderen Zellen der Tumorumgebung beeinflusst wird (Abbildung 2).
Zielgerichtete Therapie gegen den EGFR bei Darmkrebs als neuartiger Ansatz zur Vorhersage und Verbesserung der Tumorimmunogenität und Reaktion auf Checkpoint-Inhibitoren
Trotz des großen Erfolgs von Checkpoint-Inhibitoren für die Krebsbehandlung sprechen viele Patient:innen, zum Beispiel Patient:innen mit Mikrosatelliten-stabilem metastasiertem Darmkrebs (mCRC), aus Gründen, die kaum verstanden werden, nicht an. Die Standardtherapie für mCRC mit Wildtyp-RAS ist die Hemmung des EGFR in Kombination mit einer Chemotherapie. Etwa die Hälfte der Patient:innen profitieren jedoch aus unbekannten Gründen nicht von dieser Therapie.
Unter Verwendung von gentechnisch veränderten Mausmodellen (GEMM) identifizierten wir eine tumorfördernde Rolle von EGFR-exprimierenden myeloischen Zellen bei CRC und konnten zeigen, dass EGFR-positive myeloische Zellen ein schlechter Prognosefaktor für mCRC-Patient:innen sind. Wir nehmen daher als Hypothese an, dass EGFR-exprimierende myeloische Zellen einen pro-tumorigenen Phänotyp annehmen, indem sie eine immunsuppressive Umgebung schaffen. Die EGFR-Blockade könnte dies daher rückgängig machen, indem sie die Immunität gegen Tumore erhöht und die Wirksamkeit von Checkpoint-Inhibitoren verstärkt.
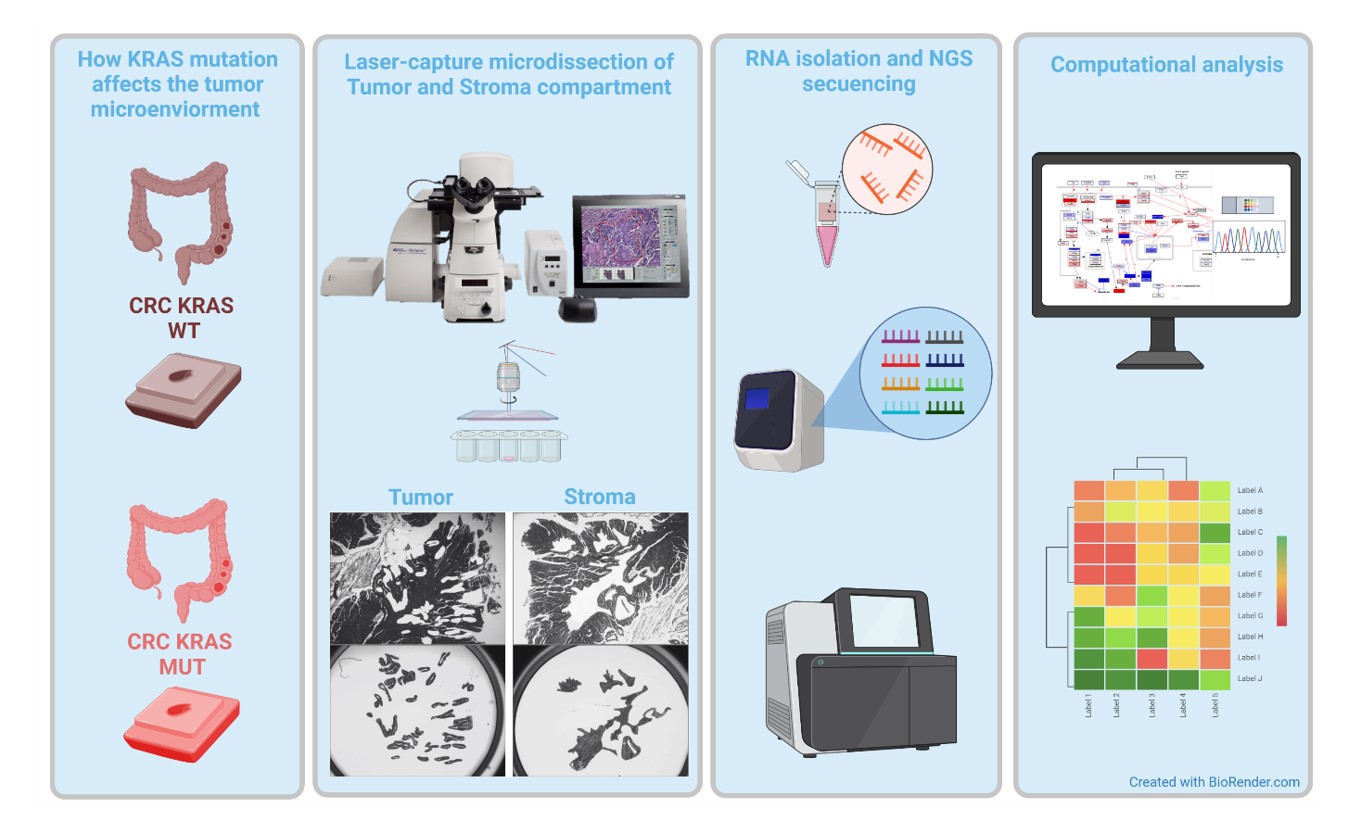
Wir haben daher eine Gruppe von Expert:innen aus den Bereichen Onkologie, Bioinformatik und Molekularbiologie zusammengestellt, um diese Hypothese zu testen, indem wir GEMM von CRC ohne EGFR in verschiedenen Zellen in Kombination mit Maus- und Humansequenzierung der nächsten Generation von Tumor-, Stroma- und Immunzellpopulationen einsetzen (Abbildung 3). Das komplexe Zusammenspiel zwischen Mutationen in Tumorzellen und Stroma wird durch Untersuchungen an großen Patient:innenkohorten in Kombination mit mechanistischen Studien in GEMM angegangen. Wir erwarten, Faktoren zu identifizieren, die Mikrosatelliten-stabilen CRC-Patient:innen Resistenz gegen eine Immuntherapie verleihen, mit dem Ziel, die Präzisionsonkologie bei mCRC zu verbessern.
Verständnis der Ursachen für die Nebenwirkungen der anti-EGFR Therapie in Krebspatienten
Die Mehrheit der Krebspatient:innen, die Anti-EGFR-Therapien erhalten, entwickelt auch eine schwere Hautentzündung, die positiv mit dem Ansprechen auf die Anti-Krebs-Behandlung korreliert. Mäuse, denen EGFR in der Epidermis fehlt, entwickeln schwere Haarfollikeldefekte und Hautentzündungen, ähnlich denen, die bei Patient:innen beobachtet wurden, die Anti-EGFR-Therapien erhielten.
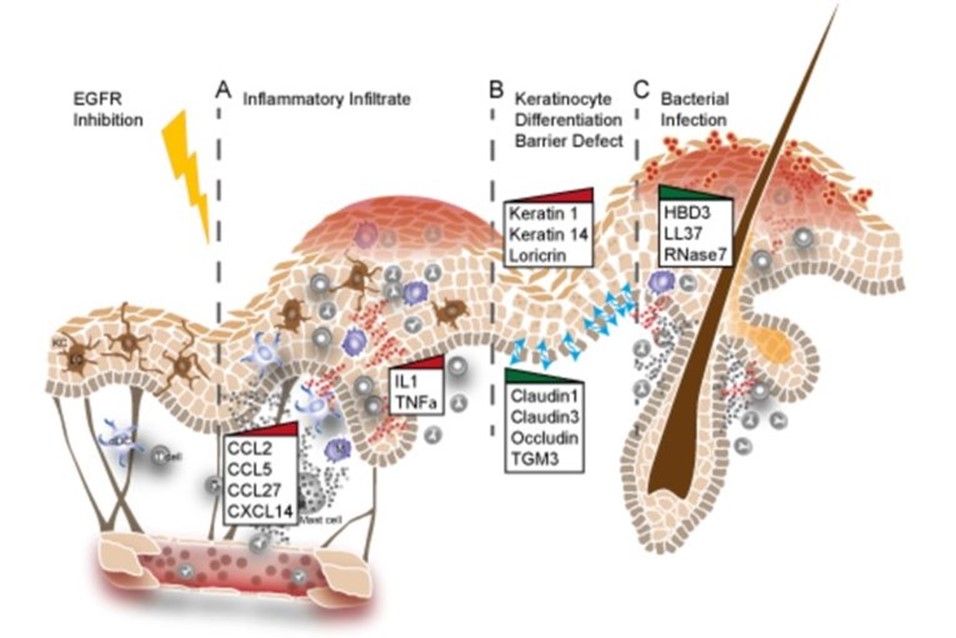
Anhand von GEMMs und Hautproben von Patient:innen konnten wir zeigen, dass die EGFR-Hemmung zur Hochregulierung von entzündlichen Zytokinen und zum Zusammenbruch der Hautbarriere führt (Abbildung 4) (Klufa et al. Sci Transl Med. 2019 Dec 11;11(522), (Lichtenberger, Holcmann, Gerber et al. Sci Transl.Med. 2013 Aug 21;5(199)). Ein tiefgreifendes Verständnis der molekularen Mechanismen, die diesen Defekten zugrunde liegen, sowie des Beitrags der verschiedenen Zelltypen im Haarfollikel werden wesentlich dazu beitragen, Strategien zu entwickeln, die darauf abzielen, die Nebenwirkungen von Patient:innen zu lindern, die Anti-EGFR-Medikamente erhalten.
Funktion dendritischer Zellen bei der Tumorentstehung und Hautentzündung
GEMMs werden von uns auch eingesetzt, um die Rolle bestimmter angeborener Immunzellen, plasmazytoiden dendritischen Zellen (pDC) sowie konventionellen (c)DC, bei Entzündungen und Krebs zu analysieren, mit dem Ziel, therapeutische Interventionsstrategien zur Stärkung der angeborenen Immunität gegen Tumore zu finden.
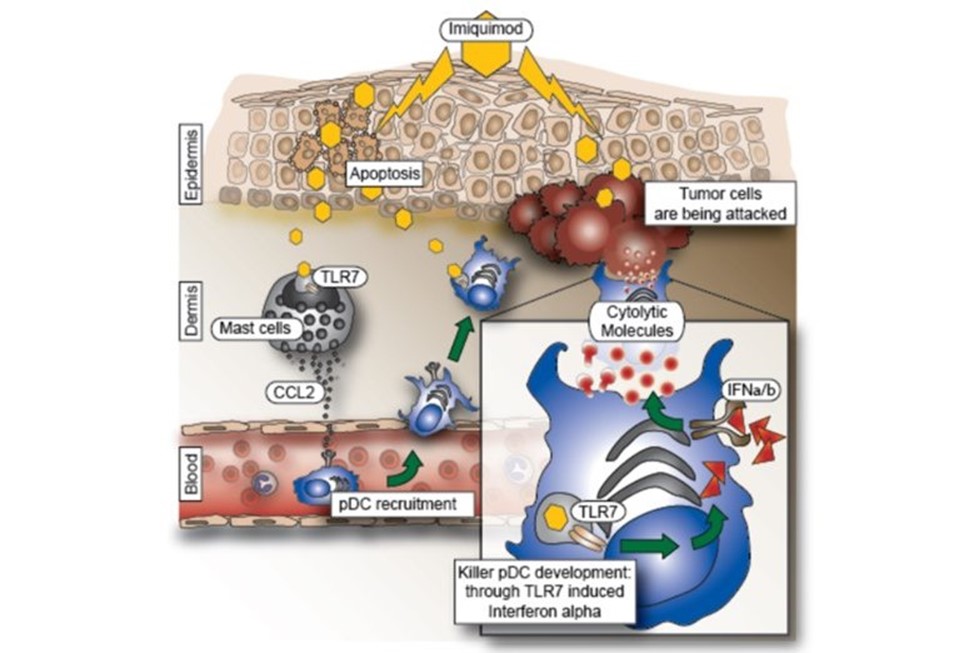
Wir entdeckten, dass wenn pDC durch Imiquimod, einen Toll-like-Rezeptor (TLR) 7/8-Agonisten, der in der Klinik zur Behandlung von Basalzellkarzinomen verwendet wird, aktiviert werden, sie in „Killerzellen“ umgewandelt werden können, die in der Lage sind, Tumore ohne Hilfe des adaptiven Immunsystems zu beseitigen (Drobits et. al. JCI, 2012). Daher könnten Imiquimod oder äquivalente Medikamente als nützliches Adjuvans und Immuntherapeutikum dienen, das in der Lage ist, Entzündungsreaktionen hin zu tumorhemmenden und tumortötenden Reaktionen zu verschieben (Abbildung 5).
in weiterer Folge untersuchen wir, ob pDC auch anti-Tumor Immunantowrten in anderen Organen wie z.B. Darm und Leber beeinflussen können.
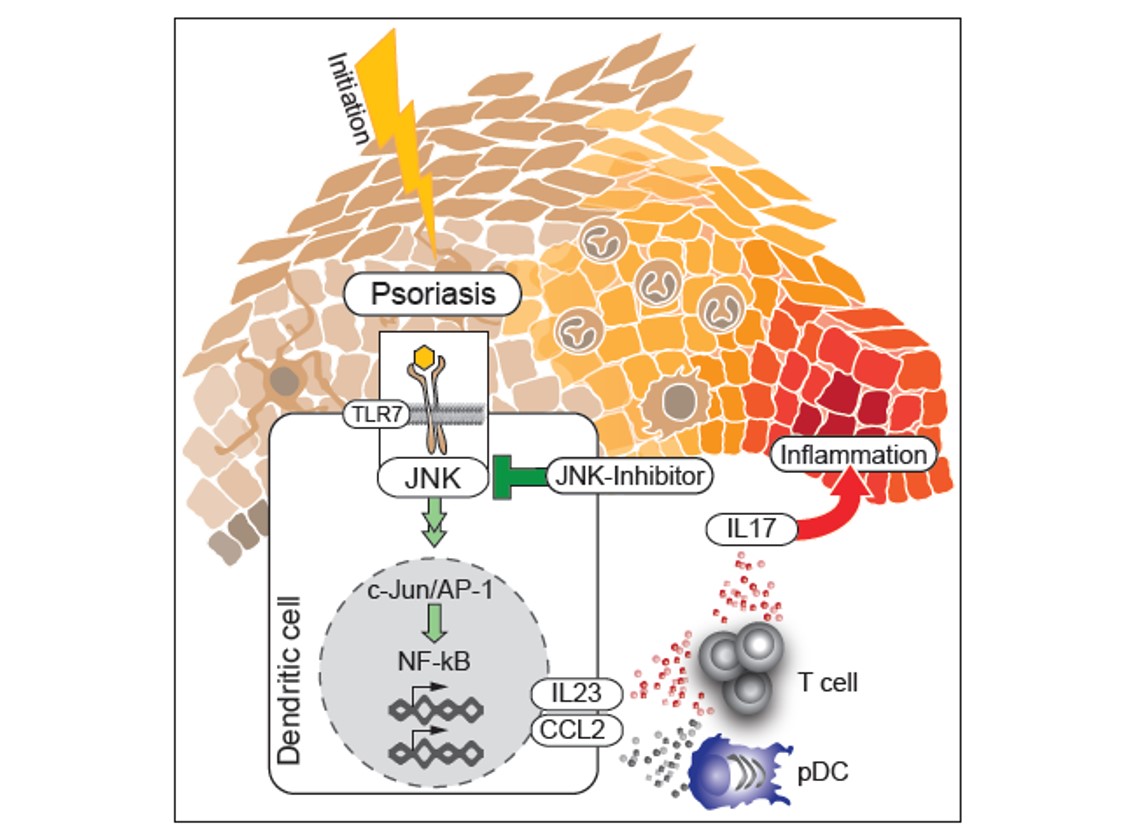
Weiters konnten wir zeigen, dass die IMQ induzierte Produktion von CCL2 durch cDC2 Zellen in der Haut über den AP-1 Transkriptionsfaktor c-jun reguliert wird. Dieser reguliert auch IL-23, ein entscheidendes Zytokin in der Entwicklung der Schuppenflechte / Psoriasis in diesen Zellen. In inflammatorischen DC in der erkrankten, nicht aber in der gesunden Haut von Psoriasispatienten konnte die Ko-expression von c-jun mit CCL2 und IL-23a gezeigt werden (Abbildung 6).
Die Hemmung von AP-1 Transkriptionsfaktoren in humanen DC führte zu einer verminderten Expression von CCL-2 und IL-23a. Solche Inhibitoren könnten daher eine neue Therapiestrategie darstellen (Novoszel et al. EMBO Mol.Med. 13, 2021).
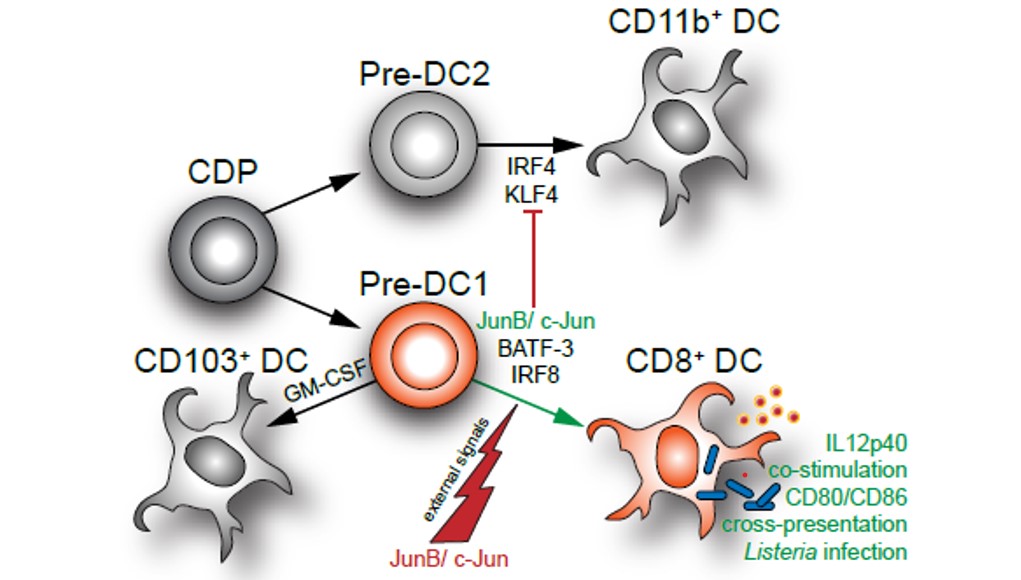
C-jun ist gemeinsam mit junB auch essentiell für die Differenzierung von DC Vorläufern in reife CD8a positive cDC1, welche für die Präsentation von Tumorantigenen eine entscheidende Rolle spielen (Abbildung 7) (Novoszel, Drobits et al. Cell Death Differ. 2021 Aug;28(8):2404-2420). In weiterer Folge untersuchen wir daher den Einfluss von AP-1 Transkriptionsfaktoren in DC auf die Tumorentwicklung in der Haut.